TỔNG HỢP CÁC DẠNG BÀI TẬP AMINO AXIT VÀ PROTEIN, CÁC DẠNG BÀI TẬP AMINOAXIT
Các dạng bài xích tập Amino Axit có đáp án cùng lời giải. Bài bác tập về Amino Axit cũng có dạng gần tương tự như bài tập về Amin. Bên cạnh dạng bài bác tập trắc nghiệm về văn bản lí thuyết còn có các bài bác tập đo lường dựa vào các phương trình phản bội ứng hóa học.
Bạn đang xem: Các dạng bài tập amino axit
Dưới đây là các dạng bài tập của Amino Axit cơ bạn dạng có lời giải và đáp án dựa trên đặc điểm hóa học, kia là: Amino axit trong phản bội ứng cùng với axit hoặc bazơ; phản nghịch ứng đốt cháy của Amino Axit để những em tham khảo.
° Dạng 1: bài xích tập tương quan phản ứng của Amino Axit với Axit với Bazơ
(Amino Axit lưỡng tính)
* Kiến thức vận dụng
• Amino axit tất cả chứa cả -COOH mang tính axit cùng –NH2 mang tính bazo nên amino axit gồm tính lưỡng tính
• giả dụ amino axit công dụng với axit thì:
m
Muối = m
Amino axit + m
Axit
• Nếu amino axit công dụng với hỗn hợp kiềm thì:
m
Muối = m
Amino axit + m
Dd kiềm – m
H2O
* bài tập 1: Amino axit X bao gồm dạng H2NRCOOH (R là cội hiđrocacbon). Cho 0,1 mol X bội nghịch ứng hết với hỗn hợp HCl (dư) thu được dung dịch cất 11,15 gam muối. Xác định công thức tên thường gọi của X?
* Lời giải:
– Đề cho: nx = 0,1(mol); m
Muối = 11,15(g);
– bản chất của Amino axit phản ứng với axit là do gốc amin, cần có:
–NH2 + H+ → NH3+ (1)
– Theo bài xích ra và theo PTPƯ ta có:
n
HCl = n
X = 0,1(mol) ⇒ m
HCl = 0,1.36,5 = 3,65(g).
– khía cạnh khác, m
Muối = mx + m
HCl ⇒ m
X = m
Muối – m
HCl = 11,15 – 3,65 = 7,5(g)
⇒ khối lượng mol phân tử X (H2NRCOOH) là:
⇒ CTPT của X là: C3H7NO2
⇒ CTCT của X có thể có là: CH3CH(NH2)COOH, H2NCH2CH2COOH.
* bài bác tập 3: Đốt cháy 8,7 gam amino axit X thì chiếm được 0,3 mol CO2 ; 0,25 mol H2O với 0,05 mol N2 (đktc). Xác minh CTPT của X?
* Lời giải:
– Áp dụng định quy định bảo toàn yếu tố ta có:
n
C = n
CO2 = 0,3 (mol).
n
H = 2n
H2O = 0,25 .2 = 0,5 (mol).
n
N = 2n
N2 = 0,05 .2 = 0,1 (mol).
m
O = m
X – m
C – m
H – m
O
⇒ m
O = 8,7 – 0,3 .12 – 0,5 . 1 – 0,1 . 14 = 3,2 (g)
⇒ n
O = 3,2/16 = 0,2 (mol)
Ta có: n
C : n
H : n
N : n
O = 0,3 : 0,5 : 0,1 : 0,2 = 3 : 5 : 1 : 2
⇒ CTPT của X là : C3H5NO2
Như vậy, bọn họ đã biết 2 dạng toán vận dụng tính lưỡng tính của Amino Axit (vừa công dụng được với axit, vừa công dụng được cùng với bazơ) với phản ứng cháy của Amino axit. Đây là nội dung cũng hay xuất hiện thêm trong nội dung đề thi tốt nghiệp THPT, bởi vì vậy, những em hãy nỗ lực ghi nhớ kỹ.
Ví dụ 3: p
H của dung dịch thuộc nồng độ mol của 3 chất H2NCH2COOH, CH3CH2COOH với CH3(CH2)3NH2 tăng theo đơn nhất tự nào dưới đây ?
A. CH3(CH2)3NH2 2NCH2COOH 3CH2COOH.
B. CH3CH2COOH 2NCH2COOH 3(CH2)3NH2.
C. H2NCH2COOH 3CH2COOH 3(CH2)3NH2.
D. H2NCH2COOH 3(CH2)3NH2 3CH2COOH.
Hướng dẫn giải đưa ra tiết:
CH3CH2COOH có môi trường thiên nhiên axit
NH2CH2COOH có môi trường trung tính
CH3(CH2)3NH2 có môi trường bazo
=> Vậy p
H của 3 chất trên được sắp tới sếp như sau:
CH3CH2COOH 2NCH2COOH 3(CH2)3NH2.
Đáp án B.
Ví dụ 4: : Cho các dãy đưa hóa : Glyxin (xrightarrow+Na
OH)X1 (xrightarrow+,,HCl,,dddoto) X2. Vậy X2 là :
A. H2NCH2COOH.
B. H2NCH2COONa.
C. Cl
H3NCH2COOH.
D. Xem thêm: Ly Bia Sư Tử Trắng Giá Rẻ, Bán Chạy Tháng 4/2023, Ly Bia Sư Tử Trắng Đại Chí Cốt Tại Hồ Chí Minh
H3NCH2COONa
Hướng dẫn giải bỏ ra tiết:
Ta tất cả phương trình làm phản ứng:
H2NCH2COOH + Na
OH → H2NCH2COONa + H2O
H2NCH2COONa + 2HCl → Cl
H3NCH2COOH + Na
Cl
Đáp án C
Dạng 2: bài xích toán về tính chất lưỡng tính của amino axit
* Một số để ý cần nhớ:
- Amino axit tất cả chứa cả -COOH mang ý nghĩa axit và –NH2 mang tính chất bazo nên amino axit có tính lưỡng tính
* nếu amino axit chức năng với axit
m muối hạt = m Amino axit + m Axit
* nếu như amino axit công dụng với hỗn hợp kiềm:
m muối hạt = m Amino axit + m dung dịch kiềm – m H2O
* một số ví dụ điển hình:
Ví dụ 1: Cho tất cả hổn hợp 2 aminoaxit no chứa 1 chức axit và 1 chức amino công dụng với 110 ml hỗn hợp HCl 2M được hỗn hợp X. Để tính năng hết với những chất trong X, phải dùng 140 ml dung dịch KOH 3M. Tổng thể mol 2 aminoaxit là :
A. 0,1.
B. 0,2.
C. 0,3.
D. 0.4.
Hướng dẫn giải đưa ra tiết:
2 amin trên có dạng NH2-R-COOH
Ta tất cả sơ đồ quá trình phản ứng như sau:
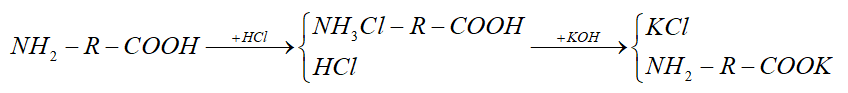
n HCl = 0,1 * 2 = 0,22 mol
n KOH = 0,14 * 3 = 0,42 mol
Áp dụng định phương tiện bảo toàn nhân tố Clo
=> n HCl = n
KCl = 0,22 (mol)
Áp dụng định công cụ bảo toàn nguyên tố K
=> n KOH = n KCl + n NH2-R-COOK
=> n NH2-R-COOK = 0,42 – 0,22 = 0,2 (mol)
=> n Amino axit = n NH2-R-COOK = 0,2 (mol)
Đáp án B.
Ví dụ 2: Hợp hóa học X là 1 a-amino axit. Mang đến 0,01 mol X chức năng vừa đầy đủ với 80 ml hỗn hợp HCl 0,125M, tiếp nối đem cô cạn hỗn hợp thu được 1,835 gam muối. Phân tử khối của X là :
A. 174.
B. 147.
C. 197.
D. 187.
Hướng dẫn giải đưa ra tiết:
n HCl = 0,08 * 0,125 = 0,01 (mol)
Áp dụng định chế độ bảo toàn khối lượng ta có:
m X + m HCl = m Muối
=> m X = 1,835 – 0,01 * 36,5 = 1,47 (gam)
Khối lượng mol của X là:
1,47 : 0,01 = 147 (gam/mol)
Đáp án B.
Dạng 3: bội phản ứng đốt cháy amino axit
* Một ví dụ điển hình:
Ví dụ 1: Khi đốt cháy hoàn toàn một amino axit X là đồng đẳng của axit aminoaxetic, nhận được . Công thức cấu trúc thu gọn hoàn toàn có thể có của X là :
A. CH3CH(NH2)COOH, H2NCH2CH2COOH.
B. H2N
C. H2N
D. kết quả khác.
Hướng dẫn giải chi tiết:
X là đồng đẳng của axit amino axetic
=> X là amino axit no, 1-1 chức mạch hở
CTPT của X bao gồm dạng: Cn
H2n+1NO2
Ta bao gồm phương trình đốt cháy:
Cn
H2n+1NO2 + O2 → n CO2 + (2n+1)/2 H2O + N2
Vì tỉ lệ thành phần về thể tích cũng chính là tỉ lệ về số mol
=> V CO2 / V H2O = n : (frac2n + 12)= 6 : 7
=> n = 3
=> CTPT của X là: C3H7NO2
CTCT của X hoàn toàn có thể có là: CH3CH(NH2)COOH, H2NCH2CH2COOH.
Đáp án A
Ví dụ 2: : Đốt cháy 8,7 gam amino axit X thì thu được 0,3 mol CO2 ; 0,25 mol H2O cùng 0,05 mol N2 (đktc). CTPT của X là :









